一种纯化17F型肺炎球菌多糖的方法与流程
一种纯化17f型肺炎球菌多糖的方法
技术领域
1.本发明属于生物制药领域,涉及一种纯化17f型肺炎球菌多糖的方法。
背景技术:
2.肺炎球菌多糖疫苗生产因为涉及多个复杂的生产过程而成本高昂,如细菌培养,荚膜多糖纯化等。因此,改进以上步骤的任一步骤都有助于提高疫苗生产成本的效益比。
3.20世纪50年代,scott首先发现十六烷基三甲基铵(ctab)对酸性多糖有较强的沉淀作用,能与多糖形成季胺络合物而沉淀多糖。十六烷基三甲基铵(ctab)是一种阳离子表面活性剂,具有从低离子强度溶液中沉淀酸性物质的特性,已经被广泛用于从多种细菌培养上清液中沉淀荚膜多糖。在高离子强度的溶液中,ctab与蛋白质和多糖形成复合物。该反应基于ctab的正电荷与cps负电荷之间的相互作用。
4.现有使用ctab沉淀17f型肺炎球菌多糖的工艺中,如美国专利需要将肺炎球菌粗裂解物进行浓缩透析,透析液使用ph值中性的磷酸盐溶液,然后向浓缩液中加入ctab以分离多糖与蛋白质、核酸等杂质,反应完成后收集沉淀,向沉淀中加入氯化钠进行解聚,然后进行后续的分离纯化。
5.本发明的创新点在于对ctab反应的工艺进行了优化,不再需要进行氯化钠解聚,简化了纯化工艺,节约了生产成本,最终收获了收率更高、质量更高的多糖。
技术实现要素:
6.本发明提出了一种简便的可放大的用于17f型肺炎球菌多糖纯化的工艺。
7.本发明在现有专利的基础上进行了改进,使用了一种全新的菌液上清透析液,不再需要进行氯化钠解聚步骤。
8.使用本工艺进行纯化,得到了纯度更高的多糖,并提高了多糖收率。
9.具体的,本发明所述的肺炎球菌多糖纯化工艺,包括以下步骤:(1)将17f型肺炎链球菌经发酵、灭活、离心、澄清后得到菌液上清;(2)将菌液上清使用截留分子量为100kd的超滤膜包进行浓缩和透析,使用中性ph值的磷酸盐缓冲溶液完成透析,透析结束后收集超滤浓缩液;(3)向超滤浓缩液中加入十六烷基三甲基溴化铵(ctab)至终浓度为1%,分离多糖与蛋白质、核酸等杂质,离心收集上清得到ctab上清液;(4)向ctab上清液中加入碘化钠(nai)至终浓度为0.5%以沉淀ctab,离心收集上清得到nai上清液;(5)将nai上清液经超滤浓缩后使用阳离子交换柱进行纯化、经超滤、冻干后收获多糖。其中,骤(2)中超滤透析液为含0.85%nacl的0.01mol/l磷酸盐缓冲液pbs,ph值为中性。其中,步骤(3)中ctab反应完成后,收集上清液,无需进行氯化钠解聚即可进行后续的碘化钠沉淀步骤。
优选的,本发明所述的肺炎球菌多糖纯化工艺,包括以下步骤:
10.(1)将肺炎链球菌经发酵、灭活、离心、澄清后得到菌液上清;
11.(2)将菌液上清使用截留分子量为100kd的超滤膜包进行浓缩和透析,使用中性ph值的含0.85%nacl的0.01mol/l磷酸盐缓冲液pbs完成透析,透析结束后收集超滤浓缩液;
12.(3)向超滤浓缩液中加入十六烷基三甲基溴化铵(ctab)至终浓度为1%,离心收集上清得到ctab上清液;
13.(4)向ctab上清液中加入碘化钠(nai)至终浓度为0.5%以沉淀ctab,离心收集上清得到nai上清液;
14.(5)将nai上清液使用截留分子量为10到100kd的超滤膜包进行浓缩和透析,透析结束后收集超滤浓缩液;
15.(6)将超滤浓缩液使用羟基磷灰石层析柱进行纯化,收集多糖流穿峰;
16.(7)将收集的多糖流穿峰使用截留分子量为10到100kd的超滤膜包进行浓缩和透析,透析溶液为注射用水(wfi),透析结束后收集超滤浓缩液;
17.(8)将透析的多糖溶液进行冷冻干燥以去除水分,得到的多糖样品用于测试,并将纯化的多糖冷冻储存。
18.对收获的多糖进行理化项目检测,具体检测方法参考《中国药典》。
19.本发明提出的纯化工艺相对于现有的纯化工艺,工艺中不再需要进行氯化钠解聚,简化了工艺,降低了生产成本,提高了生产效率。
附图说明
图1为17f工艺流程图。图2、四批次17f型肺炎球菌多糖的抗原性试验图3、17f型01批色谱图和重均分子量数据图谱图4、17f型02批色谱图和重均分子量数据图谱图5、17f型03批色谱图和重均分子量数据图谱图6、17f型04批色谱图和重均分子量数据图谱
具体实施方式
20.下面结合实施例对本发明作进一步描述,但本发明的保护范围不局限于以下所述。实施例1、肺炎球菌多糖纯化工艺(1)将肺炎链球菌经发酵、灭活、离心、澄清后得到菌液上清;(2)将菌液上清使用截留分子量为100kd的超滤膜包进行浓缩和透析,使用中性ph值的含0.85%nacl的0.01mol/l磷酸盐缓冲液pbs完成透析,透析结束后收集超滤浓缩液;(3)向超滤浓缩液中加入十六烷基三甲基溴化铵(ctab)至终浓度为1%,离心收集上清得到ctab上清液;(4)向ctab上清液中加入碘化钠(nai)至终浓度为0.5%以沉淀ctab,离心收集上清得到nai上清液;(5)将nai上清液使用截留分子量为10到100kd的超滤膜包进行浓缩和透析,透析结束后收集超滤浓缩液;
(6)将超滤浓缩液使用羟基磷灰石层析柱进行纯化,收集多糖流穿峰;(7)将收集的多糖流穿峰使用截留分子量为10到100kd的超滤膜包进行浓缩和透析,透析溶液为注射用水(wfi),透析结束后收集超滤浓缩液;(8)将透析的多糖溶液进行冷冻干燥以去除水分,得到的多糖样品用于测试,并将纯化的多糖冷冻储存。试验例1、
21.现有专利
22.(1)配制菌液上清超滤透析液为0.01mol/l磷酸盐缓冲液pb,ph值为中性;
23.(2)将肺炎链球菌经发酵、灭活、离心后得到的菌液上清进行超滤浓缩,超滤膜包截留分子量为100kd,使用超滤透析液进行透析,透析结束后收集超滤浓缩液;
24.(3)向超滤浓缩液中加入ctab,经ctab反应、离心收集沉淀、氯化钠解聚、层析、冻干后收获多糖。
25.本专利:
26.(1)配制菌液上清超滤透析液为含0.85%nacl的0.01mol/l磷酸盐缓冲液pbs,ph值为中性;
27.(2)将肺炎链球菌经发酵、灭活、离心后得到的菌液上清进行超滤浓缩,超滤膜包截留分子量为100kd,使用超滤透析液进行透析,透析结束后收集超滤浓缩液。
28.(3)向超滤浓缩液中加入ctab,经ctab反应、离心收集上清液、层析、冻干后收获多糖。
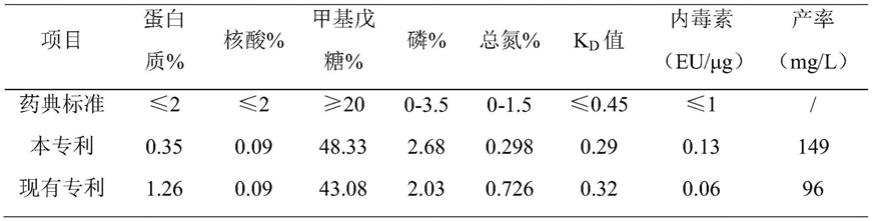
29.通过本发明工艺所获得的17f型肺炎球菌多糖各项理化指标与国家药典标准进行比较,结果如下:
[0030][0031]
可以发现,本工艺实施例所获得的17f型肺炎球菌多糖各项理化指标均符合国家药典标准,并且蛋白质、核酸、内毒素等杂质含量远低于现有专利,最终收获的多糖产量也大大提高。
[0032]
采用免疫单扩散法对本发明工艺所获得的四批次17f型肺炎球菌多糖进行抗原性试验,抗原性试验结果如图2所示。
[0034]
可以发现,本专利生产的四批次17f型肺炎球菌多糖有抗原性,均能与17f型肺炎球菌抗血清形成沉淀圈。
[0035]
对四批17f型肺炎球菌多糖抗原性试验形成的沉淀圈直径数据进行分析,结果如下:
[0036]
可以看出,四批次17f型肺炎球菌多糖产生的沉淀圈直径相近,抗原性强弱无明显差异。
[0037]
采用多角度激光散射-凝胶色谱联用仪(hpsec-malls)对4批次17型肺炎球菌多糖进行重均分子量(mw)检测,得到色谱图和重均分子量数据(多分散系数(mw/mn))如如3-图6所示:
[0039]
可以看出,17f型4批次肺炎多糖的多角度激光散射图谱峰形基本一致;4批次17f型肺炎球菌多糖重均分子量差异较小,说明分子量分布较为均匀,批间差异不大。
- 激光透明组合物和激光焊接方法...
- 一种无血干细胞培养灌流装置及...
- UBE3A基因和表达盒及其应...
- 一种新型荧光检测试剂及定量检...
- 一种化合物及其应用的制作方法
- 邻羟基苯乙酰拼接双吲哚甲基类...
- 用于有机电致发光器件的有机化...
- 一种鱼皮源医用级非变性胶原及...
- 双生病毒DNA1分子诱导可遗...
- 斑螯素和生物活性斑螯素衍生物...
- 还没有人留言评论。精彩留言会获得点赞!